سایکوبیوتیکها، که به عنوان یک حوزه نسبتا جدید در زمینه تغذیه و روانشناسی شناخته میشوند، مربوط به استفاده از پروبیوتیکها و پریبیوتیکها برای بهبود سلامت روانی هستند. این مفهوم بر اساس فرضیهای است که رابطه مهمی بین روده و مغز وجود دارد، به طوری که تغییر در میکروبیوم روده میتواند بر سلامت روانی تأثیر بگذارد.
پروبیوتیکها شامل باکتریهای زندهای هستند که میتوانند فواید سلامتی داشته باشند وقتی به مقدار کافی مصرف شوند، در حالی که پریبیوتیکها مواد غذایی هستند که توسط میکروبهای مفید در روده تجزیه میشوند.
تحقیقات در این زمینه نشان دادهاند که تغییرات در میکروبیوم روده ممکن است با بیماریهایی مانند افسردگی، اضطراب، و اختلالات خوردن مرتبط باشد. در مجموع، سایکوبیوتیکها نشان میدهند که تغذیه و سلامت روده میتوانند عناصر مهمی در مدیریت و درمان برخی از اختلالات روانی باشند.
تعریف سایکوبیوتیک
بر اساس اعلام “انجمن روانپزشکی بیولوژیکی”، اصطلاح “روانبیوتیکها” یا “سایکوبیوتیک ها” به عنوان “ارگانیسم های زندهای که مصرف آن به مقدار کافی، برای بیمارانی که از بیماریهای روانی رنج میبرند، فواید سلامتی ایجاد میکند” تعریف میشود. تصور می شود که این باکتری های پروبیوتیک اثرات مفید خود را بر سلامت روان و خلق و خو به روش های مختلف اعمال می کنند. بر اساس مطالعات انجام شده روانبیوتیکها میتوانند در موارد زیر نقش داشته باشند:
- تولید مواد شیمیایی عصبی مانند سروتونین و گاما آمینوبوتیریک اسید (GABA) که خلق و خوی ما را تعدیل می کنند.
- فعال کردن مسیرهای عصبی بین روده و مغز
- محدود کردن تولید سیتوکین های التهابی (مولکول های سیگنال دهنده سلولی)، کاهش التهاب در بدن و مغز
- بهبود وضعیت تغذیه عمومی
- کاهش باکتری های بیماری زا (بد) در روده ها، که می تواند بسیاری از مشکلات سلامتی را در بقیه بدن ایجاد کند.
بنابراین، بر خلاف اکثر درمانهای پزشکی آلوپاتیک، این باکتریهای مفید شیوههای عمل متفاوت دارند. آنها به طرق مختلف بر خلق و خو و سلامت روان ما تأثیر می گذارند و به آنها پتانسیل زیادی را به عنوان یک ابزار درمانی برای اختلالات سلامت روان می دهند.
تاثیر سلامت روده بر وضعیت روانی
تأثیر سلامت روده بر وضعیت روانی یک حوزه تحقیقاتی در حال رشد است که بخشی از مطالعهای بزرگتر به نام “محور روده-مغز” است. این محور به تعاملات پیچیده بین سیستم گوارشی و سیستم عصبی مرکزی اشاره دارد. در اینجا چند جنبه کلیدی از این تعاملات آورده شده است:
- میکروبیوم روده: روده انسان خانهای برای تریلیونها میکروارگانیسم است، از جمله باکتریها، ویروسها و قارچها. این میکروارگانیسمها، معروف به میکروبیوم، نقش مهمی در سلامتی انسان دارند. تحقیقات نشان میدهند که تعادل میکروبیوم روده میتواند بر خلق و خو و رفتار تأثیر بگذارد.
- سیگنالینگ روده-مغز: روده و مغز از طریق یک شبکه پیچیده از سیگنالها که شامل مسیرهای عصبی، هورمونی و ایمنی است، با هم در ارتباط هستند. برای مثال، سیستم عصبی معوی (مغز دوم) به طور مستقیم با مغز ارتباط برقرار میکند.
- نقش پروبیوتیکها و پریبیوتیکها: پروبیوتیکها (میکروارگانیسمهای زنده که ممکن است فواید سلامتی داشته باشند) و پریبیوتیکها (مواد غذایی که میکروبهای مفید روده را تغذیه میکنند) میتوانند بر سلامت روده و به طور بالقوه بر سلامت روان تأثیر بگذارند.
- تأثیرات روده بر خلق و خو و اختلالات روانی: مطالعات نشان دادهاند که اختلال در تعادل میکروبیوم روده میتواند با شرایطی مانند افسردگی، اضطراب و حتی اختلالات طیف اوتیسم مرتبط باشد.
- مداخلات درمانی: با توجه به ارتباط بین روده و مغز، درمانهایی که بر بهبود سلامت روده تمرکز دارند، مانند تغییر در رژیم غذایی، مصرف پروبیوتیکها و پریبیوتیکها، میتوانند برای درمان برخی اختلالات روانی مورد بررسی قرار گیرند.
در حالی که این حوزه تحقیقاتی هنوز در مراحل اولیه قرار دارد، افزایش شواهد نشان میدهد که سلامت روده میتواند تأثیر قابل توجهی بر سلامت روانی داشته باشد. این موضوع باز میگردد به این نکته که رویکردهای جامع و چند وجهی به سلامتی، که شامل توجه به تغذیه و سلامت روده میشود، میتواند در مدیریت و درمان اختلالات روانی مؤثر باشد.
مطالعات انسانی انجام شده در حوزه سایکوبیوتیک ها
مطالعات سایکوبیوتیک ها در دو دسته حیوانات مدل و مطالعات انسانی طبقه بندی میشوند. مطالعات انجام شده روی حیوانات مدل اغلب تاثیرات اثبات شده و مورد تاییدی را نشان داده اند. مطالعات انسانی به دلیل مسائل اخلاقی و همچنین پیچیده بودن صفات سایکولوژیک انسانی محدودتر بوده، اما با این وجود نتایج جالبی داشته اند. در ادامه مرور کوتاهی بر برخی مطالعات انسانی انجام شده خواهیم داشت :
- تاثیر Lactobacillus casei Shirota به عنوان یک سایکوبیوتیک: در یک مطالعه با شرکتکنندگان مرد و زن (124 نفر)، مصرف یک نوشیدنی شیری تخمیر شده حاوی لاکتوباسیلوس کازئی شیروتا یا دارونما مورد بررسی قرار گرفت. در پایان سه هفته، تغییر چشمگیری در خلق و خوی خودگزارشی مشاهده نشد. با این حال، در میان شرکتکنندگانی که امتیازات خلق و خوی پایهشان در پایینترین سوم کل محدوده قرار داشت، مکملهای پروبیوتیک باعث شد که تعداد بیشتری از شرکتکنندگان خود را خوشحالتر از افسرده برخوردار کنند.
- مطالعه لاکتوباسیلوس هلوتیکوس و بیفیدوباکتریوم لانگوم به عنوان سایکوبیوتیک: در یک طرح تصادفی و دوسوکور، شرکتکنندگان سالم (55 نفر) یا مخلوطی از پروبیوتیکها (Lactobacillus helveticus R0052 and Bifidobacterium longum) یا دارونما را برای 30 روز مصرف کردند. نتایج نشان داد که شرکتکنندگانی که پروبیوتیکها را مصرف کردند، کاهش قابل توجهی در خلق و خوی منفی و استرس خود را گزارش کردند.
- مطالعه مخلوط چندین پروبیوتیک و تاثیر آن در ویژگی خلق و خو: در یک آزمایش کنترلشده تصادفی، شرکتکنندگان سالم (40 نفر) یا محصول دارونما یا مخلوطی از چندین پروبیوتیک (Bifidobacterium bifidum W23, Bifidobacterium lactis W52, Lactobacillus acidophilus W37, Lactobacillus brevis W63, Lactobacillus casei W56, Lactobacillus salivarius W24, and Lactococcus lactis W19 and W58) را برای 4 هفته مصرف کردند. این مطالعه نشان داد که مصرف پروبیوتیکها باعث کاهش واکنش به خلق و خوی غمگین میشود.
- لاکتوباسیلوس کازئی شیروتا و استرس تحصیلی: در یک مطالعه جالب، دانشجویان سالم (47 نفر) قبل از امتحان پزشکی، لاکتوباسیلوس کازئی شیروتا یا دارونما را برای 8 هفته مصرف کردند. نتایج نشان داد که گروه پروبیوتیک کورتیزول پلاسما پایینتری نسبت به گروه دارونما داشت.
- تاثیر سایکوبیوتیک ها در سندرم روده تحریک پذیر: در یک مطالعه در افراد مبتلا به سندرم روده تحریکپذیر، مصرف لاکتوباسیلوس سالیواریوس UCC4331 و بیفیدوباکتریوم اینفانتیس 35624 مورد بررسی قرار گرفت. تنها شرکتکنندگانی که بیفیدوباکتریوم اینفانتیس 35624 مصرف کردند، تغییرات مثبت در نسبت سیتوکینها را نشان دادند.
این تحقیقات تنها بخشی از تحقیقات روی سایکوبیوتیک ها هستند و سالهای اخیر مطالعات زیادی روی این گروه از باکتری ها انجام شده است.
تاثیر سایکوبیوتیک ها بر مسیرهای سیگنالینگ مغزی
مکانیسمهایی که روانبیوتیکها از طریق آن اثرات خود را اعمال میکنند، هنوز به وضوح تعریف نشدهاند و به خوبی شناخته نشدهاند. اگرچه برخی مطالعات وجود دارد که بینش مکانیکی را برای انسان فراهم می کند، اکثر تحقیقات بر اساس مدل های جوندگان است. یک گام مهم در توسعه دانش مکانیسم ها در بررسی چگونگی ارتباط میکروبیوم و مغز با یکدیگر است.
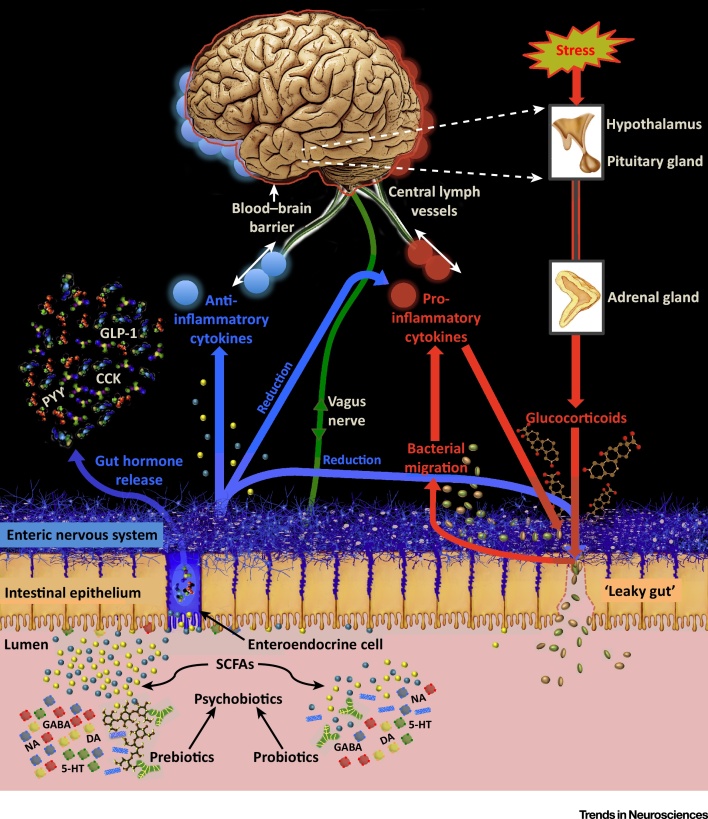
پروبیوتیک ها به طور مستقیم باکتری های مفیدی مانند لاکتوباسیل ها و بیفیدوباکتری ها را وارد روده می کنند. پری بیوتیک ها (به عنوان مثال، گالاکتو-الیگوساکاریدها) از رشد چنین باکتری هایی حمایت می کنند.
SCFA و هورمون های روده: هم پروبیوتیک ها و هم پری بیوتیک ها تولید اسیدهای چرب با زنجیره کوتاه (SCFAs) را افزایش می دهند که با سلول های غدد درون ریز مخاط روده تعامل می کنند و ترشح هورمون های روده مانند کوله سیستوکینین (CCK)، پپتید تیروزین تیروزین (PYY) و GLP-1 را کاتالیز می کنند. ممکن است پری بیوتیک ها در این زمینه در مقایسه با پروبیوتیک ها اثرات قوی تری داشته باشند. SCFA ها و هورمون های روده وارد گردش خون می شوند و می توانند به سیستم عصبی مرکزی مهاجرت کنند. هورمون های روده نیز توسط بافت هایی غیر از سلول های غدد درون ریز ترشح می شوند.
انتقال دهنده های عصبی: روانگردان ها تولید انتقال دهنده های عصبی را در روده افزایش می دهند، از جمله دوپامین (DA)، سروتونین (5-HT)، نورآدرنالین (NA) و γ-آمینوبوتیریک اسید (GABA)، که احتمالاً انتقال عصبی را در سیناپس های پروگزیمال سیستم عصبی روده تعدیل می کنند.
اتصالات واگ: عصب واگ روی نورون های روده سیناپس می کند و ارتباط روده و مغز را امکان پذیر می کند. استرس، عملکرد مانع و سیتوکین ها: اختلال عملکرد سد از طریق قرار گرفتن در معرض گلوکوکورتیکوئید ناشی از استرس تشدید می شود. این امر مهاجرت باکتری ها را با اجزای پیش التهابی امکان پذیر می کند، التهاب را مستقیماً افزایش می دهد و همچنین باعث افزایش سیتوکین های پیش التهابی از طریق پاسخ ایمنی می شود. این سیتوکین ها یکپارچگی سد خونی مغزی را مختل می کنند و اجازه دسترسی به عناصر بالقوه بیماری زا یا التهابی را می دهند.
سیتوکین های پیش التهابی (دایره های قرمز) نیز یکپارچگی سد روده را کاهش می دهند. عملکرد روانبیوتیک عملکرد سد روده را بازیابی میکند و غلظت گلوکوکورتیکوئیدها و سیتوکینهای پیش التهابی در گردش را کاهش میدهد. آنها همچنین غلظت سیتوکین های ضد التهابی (دایره های آبی) را افزایش می دهند که یکپارچگی سد خونی مغزی، سد روده را افزایش می دهد و التهاب کلی را کاهش می دهد. سیتوکین هایی که در مغز جمع شده اند، نشان دهنده تعامل سیتوکین با سد خونی مغزی است. رگهای لنفاوی مرکزی: سیتوکینها ممکن است مستقیمتر از آنچه قبلاً از طریق عروق لنفاوی مرکزی کشف شده بودند، مستقیماً با مغز تعامل داشته باشند.
منبع : Psychobiotics and the Manipulation of Bacteria–Gut–Brain Signals
برهمکنش روان بیوتیک ها و اعصاب دستگاه گوارش
باکتریهای روده بر آستانههای الکتروفیزیولوژیک در نورونهای سیستم عصبی رودهای تأثیر میگذارند. به عنوان مثال، نورونهای ماینتریک که در معرض مواد تخمیر شده توسط بیفیدوباکتریوم لانگوم NCC3001 قرار گرفتهاند، در پاسخ به تحریک الکتریکی، تولید پتانسیل عمل کمتری نشان دادند. به طور مشابه، نورونهای AH کولونیک (نورونهای حسی اصلی در کولون) که با لاکتوباسیلوس رامنوسوس تیمار شدهاند، افزایش قابلیت تحریکپذیری را نشان دادند، اثری که از مهار دروازههای پتاسیم کنترل شده توسط کلسیم ناشی میشود. مطالعات دیگر نشان دادهاند که نورونهای گانگلیون ریشهی دورسال در کولون در پاسخ به تحریک ناخوشایند، هایپراکسیتابیلیتی (تحریکپذیری بیش از حد) نشان نمیدهند اگر با لاکتوباسیلوس رامنوسوس تیمار شده باشند. همچنین، نورونهای ماینتریک در نزدیکی لومن روده قرار دارند، که ارتباط آنها با میکروبیوم را تسهیل میکند. در موشهای عاری از میکروب، این نورونها سطح پایینتری از تحریکپذیری را نسبت به همتایان عادی خود نشان میدهند. یک مطالعه شواهدی از ناهنجاریهای عصبی روده در جیجونوم و ایلئوم موشهای عاری از میکروب در مقایسه با کنترلها یافت، با موشهای عاری از میکروب که تراکم اعصاب کمتری، اعصاب کمتری در هر گانگلیون و تعداد بیشتری از نورونهای نیترژنیک ماینتریک را نشان میدادند. شواهد اخیر همچنین نشان میدهد که میکروبیوم بر انتقال یونها تحت کنترل سیکلیک آدنوزین مونوفسفات (cAMP) تأثیر میگذارد.
در مجموع، این نتایج شواهد قابل توجهی از تعدیل مستقیم و باکتریزده سیستم عصبی رودهای را ارائه میدهند. علاوه بر این، تأثیر میکروبیوم بر سیستم عصبی رودهای فراتر از نورونها است، با یافتههای اخیر که نشان میدهد باکتریهای روده نقش حیاتی را در توسعه و هماستقرار جمعیتهای گلیال در روده بازی میکنند.
باکتریهای روده همچنین از طریق متابولیسم فیبرهای غیرقابل هضم، طیف گستردهای از نوروترانسمیترها را تولید میکنند. اینها شامل دوپامین و نورآدرنالین توسط اعضای خانواده باسیلوس، GABA توسط خانواده بیفیدوباکتریا، سروتونین توسط خانوادههای انتروکوکوس و استرپتوکوکوس، نورآدرنالین و سروتونین توسط خانواده اشرشیا، و GABA و استیلکولین توسط خانواده لاکتوباسیلیها تولید میشوند. هر چند هنوز شواهد مستقیمی وجود ندارد، اما احتمالاً این نوروترانسمیترها فعالیت سیناپسی در نورونهای مجاور سیستم عصبی رودهای را تنظیم میکنند، و این یک مسیر مهم برای تحقیقات آینده است.